
Spontaneous Pneumomediastinum: A Possible Severe Condition in SARS-CoV-2 Pneumonia
Jacqmin et al.
**中文内容仅供参考,一切以英文原文为准。
背景:自发性纵隔气肿(Spontaneous Pneumomediastinum, SP)是指在没有受到外部创伤的情况下,纵隔内出现游离空气,这些空气进入到肺泡外的组织中。这种状况相对罕见,但可能是重症急性呼吸综合征冠状病毒2 (SARS-CoV-2) 引发的肺炎的一种并发症。据之前的病例报告,患有COVID-19并伴有纵膈气肿的病人使用机械通气的比例较高。
病例描述:本篇文章报告了两例由COVID-19感染引起的轻、重度自发性纵隔气肿的患者及其预后。
评论:该报告的目的是回顾现有文献中关于这一现象的报道。文章探讨了这种并发症的病理机制,以及它如何反映COVID-19肺炎的严重程度。
结论:目前尚不清楚在SARS-CoV-2引发的肺炎中,自发性纵隔气肿是否是一个潜在的疾病恶化的预测因子,因为它似乎与更高的死亡率没有直接关联。
背景
自2019年12月以来,一种新型冠状病毒引发的重症急性呼吸综合征(SARS)的致命病例从中国武汉迅速扩散。在短短一年时间内,重症急性呼吸综合征冠状病毒2(SARS-CoV-2)感染的确诊病例已达到8850万例,死亡人数超过190万。
COVID-19大流行及其临床表现给医生们带来了前所未有的挑战。SARS-CoV-2肺炎最典型的影像学特征是双肺后部和下侧区域多灶性或胸膜下磨玻璃影,伴随小叶间隔间或小叶间隔内增厚。
已有文献报道了若干SARS-CoV-2肺炎患者出现自发性纵隔气肿的病例。关于这一现象确切的病理生理机制至今仍不明确。本篇文章报告两例在重症监护病房(ICU)接受治疗的COVID-19感染患者中发生的轻、重度自发性纵隔气肿。本文旨在通过回顾相关文献,探讨这种并发症的潜在病理机制,并讨论其作为恶化/非恶化预测因子的可能结果。
病例描述
病例报告1
一名49岁男性患者因连续1周出现干咳、心动过速和呼吸困难而被送往急诊室。该患者既往有高血压病史,并因多囊肾接受过肾脏移植手术,否认有吸烟和饮酒史。入院时,该患者在室内空气中的氧饱和度为93%,体温为37.2°C,血压为140/97 mmHg,脉搏为92次/分。
经过基本血液检查后,发现该患者C反应蛋白轻度升高(11.8 mg/L,参考值:<5 mg/L)。血细胞计数显示白细胞数量在正常范围内,为4.12×10^3/μL(参考值:3.7–9.5×10^3/μL),淋巴细胞数量减少,为1.6×10^3/μL(参考值:1.2–4.7×10^3/μL),血清乳酸脱氢酶(LDH)升高至261 U/L(参考值:87–241 U/L)。通过鼻咽拭子的实时定量逆转录聚合酶链反应(RT-PCR)检测确认了SARS-CoV-2感染。
胸部计算机断层扫描(CT)无对比显示:肺实质受影响体积中,中度弥漫性肺泡损伤程度约为20%。当时并未发现气胸或纵隔气肿。
患者被收治到内科病房后,接受了10天的口服皮质类固醇治疗,并皮下注射了预防剂量的低分子量肝素。患者第五天还通过高流量鼻导管(Optiflow)以60 L/分的流速接受了氧气治疗,吸入氧浓度(FiO2)为80%。氧疗第二天,患者因呼吸衰竭需机械通气,被转入重症监护室(ICU),胸部CT观察到严重的自发性纵隔气肿,伴有广泛的颈部皮下气肿和心脏移位(►见图1)。此外,评估发现肺部损伤范围增加(总肺容量的75%受累)。随后患者出现了血流动力学不稳定,需要增加使用正性肌力药物。通过支气管镜检查排除了气管或支气管破裂的可能。未发现其他导致纵隔气肿的次要原因。
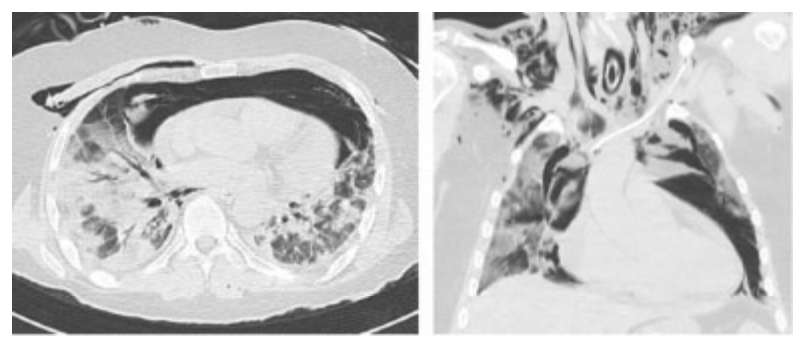
图1. 胸部CT轴向和冠状面图像显示纵隔气肿的范围以及在SP进展中的心脏移位,沿着主支气管朝向心尖。SP,自发性纵隔气肿。
经过多学科讨论,即使患者并非典型的气胸症状,考虑到患者的危急状态,仍决定执行右侧缩小纵隔切开术(在右侧第二肋间隙旁的切口),以分解前纵隔分离的软组织和脂肪组织,并实现胸腔引流。手术在ICU收治后的第12天进行,从临床和影像学改善方面证明有效(►见图2);患者在24小时内逐渐停用了支持药物并拔出胸腔引流管。
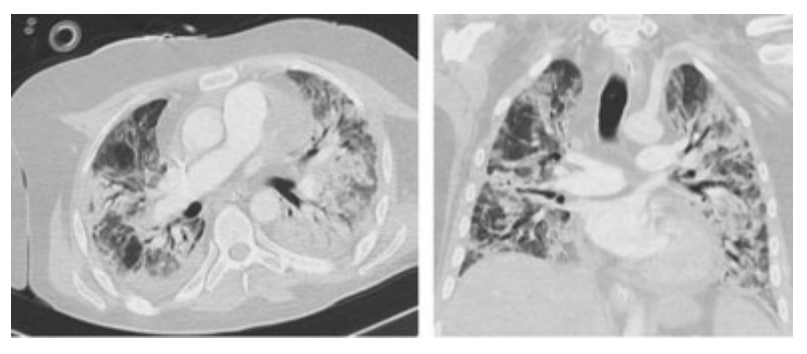
图2. 纵隔切开术后的胸部CT轴向和冠状面图像,纵隔气肿几乎完全消失。
不幸的是,患者的状况在几天后再次恶化,并在第21天因呼吸衰竭去世。
病例报告2
一名76岁男性患者连续4天出现呼吸困难,血氧饱和度持续下降,由家庭医生转诊至急诊室。该患者并未表现出咳嗽症状。在他的病史中,唯一值得注意的是高血压。患者入院时体温为37.8°C,心率为173次/分。血液检查显示C反应蛋白水平显著升高,至174 mg/L,并伴有淋巴细胞减少。RT-PCR检测呈阳性,胸部CT扫描显示肺部实质受损范围达50%,表现为严重的肺泡损伤。
患者入院后被收治入ICU共计11天,随后被转移至中护病房,并接受氧流量为60 L/分、FiO2为60%的鼻部高流量吸氧装置治疗。
患者入院第17天,由于呼吸功能进一步恶化,再次被收入ICU。病情加重期间,进行了胸部CT扫描,结果显示患者出现自发性纵隔气肿(SP)(►见图3)。随后,患者接受了为期5天的插管和机械通气治疗。
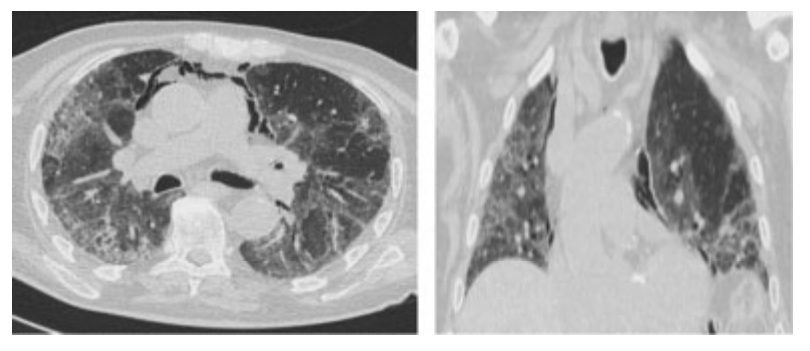
图3. 第二位SARS-CoV-2肺炎并发自发性纵隔气肿患者的胸部CT轴位和冠状位图像。SARS-CoV-2,即冠状病毒2引发的重症急性呼吸综合征。
在该病例中,患者接受了保守治疗,几天之内SP逐渐好转。随着纵隔气肿减轻,患者的整体状况也逐步改善,共在ICU停留29天。经过两个月的住院治疗和呼吸康复训练,患者最终得以出院(►见图4)。
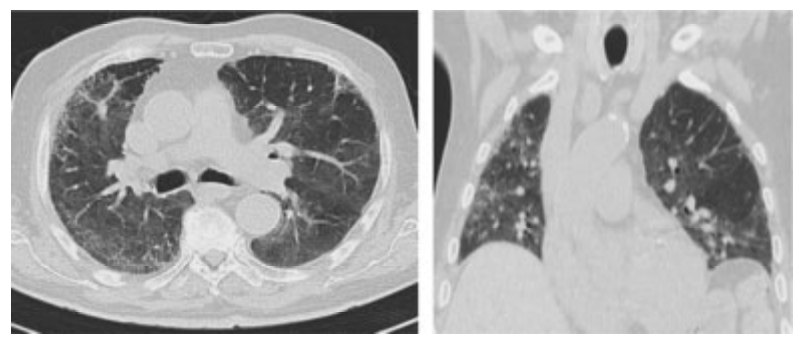
图4. 初次发病2个月后的随访胸部CT轴位和冠状位图像,显示纵隔气肿完全吸收。
评论
纵隔气肿(SP)是指气体释放到肺泡外组织中,通常是由于肺泡破裂所致:游离气体从破裂的肺泡夹层沿支气管血管鞘渗漏至肺门和纵隔。这一病理生理过程最初由Macklin在1939年描述,并称为“Macklin效应”。Macklin效应在胸部CT上表现为与支气管血管鞘相连的线性空气聚集。
慢性阻塞性肺疾病、哮喘以及侵袭性机械通气期间的肺部气压伤是引起SP的主要危险因素。然而,SP也是感染性肺炎的一种罕见并发症。
• 在免疫力正常的宿主中,SP并不常见,它可能作为葡萄球菌或真菌肺炎的并发症出现。也有报道称,继发于系统性红斑狼疮的间质性肺炎也可能导致SP。
• 在免疫功能低下的患者中,SP可见于卡氏肺囊虫肺炎、肺结核或巨细胞病毒性肺炎。
自COVID-19大流行以来,已有少数与SARS-CoV-2相关的SP被报道。虽然其机制尚不清楚,但推测其原因为SARS-CoV-2会引起咳嗽/Valsalva动作以及通气相关的弥漫性肺泡损伤,进一步导致肺泡内压力增加以及气压伤,从而引发SP。在收入ICU之前,该患者经历了强烈的反复干咳,但SP的影像学证据是在患者插管和机械通气后发现的。
SP通常在呼吸道症状发作后的第20天(19.6±4.6)观察到。
在SP患者中一致观察到血清LDH水平显著升高。病毒载量或皮质类固醇的累积剂量通常与SP无关。导致SP的肺泡损伤似乎与病毒载量和细胞溶解无关,它可能是严重弥漫性肺泡损伤的结果,并且可能与间质性肺气肿有关。考虑到这种情况在COVID-19肺炎中大约在第20天开始出现,除了病毒诱导的细胞溶解之外的其他过程可能与其病理途径相关。宿主中的重要免疫反应也可能是SP发作的原因之一。
通常,纵隔气肿(SP)对保守治疗有良好的反应,通过降低通气压力和密切监测即可消解。极少数情况下,患者会发展为张力性纵隔气肿,在这种情况下应立即对患者施行纵隔切开术和胸腔引流。正如病例1中所述,当患者出现与游离气体释放导致胸内压力增加相关的纵隔移位,并伴有血液动力学不稳定时,可能需要对其进行单侧或双侧胸腔引流。在这种情况下,结合采用简化的纵隔入路(即通过位于第二肋间隙水平的小型胸骨旁切口)可能是一个较好的处理方案。实际上,严重的SP会减少静脉回流,并且影响前负荷,使心输出量减少,若不进行治疗,可能会导致患者死亡。在这种情况下,基于CT和临床评估,我们认为必须快速执行胸腔/纵隔引流。引流可在几小时内使胸腔内压恢复至最佳状态,并且使心脏的移位和血液动力学参数恢复正常。伴有肺塌陷的张力性气胸也是立即放置胸腔导管的明确指征。若伴有显著的颈部和面部皮下气肿同样需要进行胸腔引流(►表1)。

表1. 胸膜切开引流术的手术指征
作者从文献中总结了13例在SARS-CoV-2肺炎中患有SP的患者(►表2)。在COVID-19肺炎中,关于轻度/重度SP的报告或描述相当罕见,因为即使在SARS-CoV-2大流行期间,这种病理表现也并不常见,而且患者通常需要机械通气治疗。在我们的回顾中,除了一名患者外,所有SP病例都采用了保守治疗。到目前为止,还没有关于SARS-CoV-2肺炎中胸腔/纵隔开放式管理SP的数据记录。这可以归因于许多作者用CT扫描描述的“严重”SP实际上只是轻度到小型的纵隔气肿,不会像本文病例1中描述的那样有引起严重的心脏-纵隔移位的风险,该病例中的严重SP患者是极为罕见的。
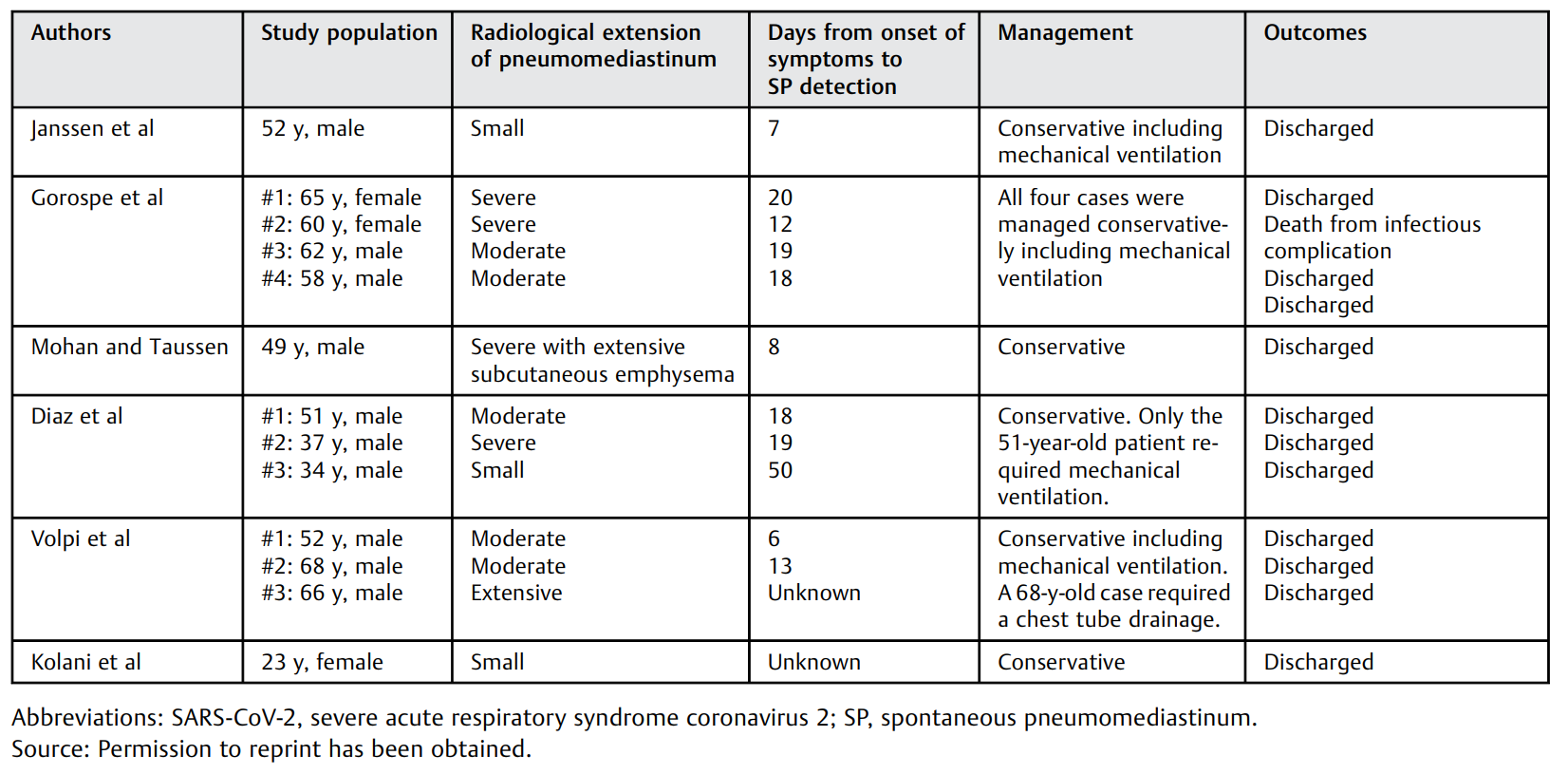
表2. 6例报告中SARS-CoV-2肺炎患者及SP患者
一些报道证实,COVID-19患者的SP是插管和死亡的危险因素。►表2中显示了其更高的插管率,但更高的死亡率有被高估的可能。
研究表明,“中度或轻度”SP完全消解需要大概28天的时间。可以推测,COVID-19肺炎中的纵隔气肿是在长期且严重的病程中观察到的。
总之,自发性纵隔气肿在SARS-CoV-2肺炎中是一种罕见并发症,可能与较高的插管/机械通气率有关,但似乎与文献中描述的更高的死亡率无关。如果保守治疗不充分,可以选择使用外科手术治疗特定患者。仍需要进一步的研究来评估这种COVID-19肺炎的潜在并发症是否是疾病恶化的指标。
点评
本文通过调查新型冠状病毒(SARS-CoV-2)肺炎患者中自发性纵隔气肿(SP)的发生情况,探讨其与疾病严重程度的关系。通过报告两例COVID-19感染患者出现SP的病例,描述了COVID-19感染患者中自发性纵隔气肿的发生情况,并分析了这种并发症的病理机制和可能预后。作者还回顾了相关文献,讨论了SP在COVID-19肺炎中的严重性和预后的关联。通过对这些问题的探究,增加了对COVID-19肺炎并发症的理解,并为临床医生提供了更多关于患者预后和治疗策略的信息,有助于改善COVID-19患者的综合治疗和管理。
本期中文解读
于皓月
/初稿
郑子龙
/初审
范成铭
/校审
范成铭,博士
The Thoracic and Cardiovascular Surgeon 编委
中南大学湘雅二医院
外科学博士,药学博士后,副研究员,博士研究生导师,中南大学湘雅二医院心血管外科主治医师,中华志愿者协会中西医结合专家志愿者委员会心外科专业组常务委员,中国研究型医院学会心脏瓣膜病专业委员会青年委员,湖南省医学会胸心血管外科学专业委员会青年委员,美国阿拉巴马大学伯明翰分校生物医学工程学系国家公派联合培养博士,中南大学十佳大学生、中南大学湘雅二医院青年岗位能手、十佳青年、湖南省卫生健康高层次人才,中南大学“升华学者计划”优秀青年人才。美国胸外科协会(AATS) Evarts A. Graham Memorial Traveling Fellowship 2023年获得者(首位获得该奖项的国内心外科医生,每年仅资助一名心外科医师)。美国Samuel and Jean Frankel心血管中心Fellow。荷兰Catharina医院心胸外科Fellow,比利时Cliniques universitaires Saint-Luc医院心胸血管外科Fellow。主持国家自然科学基金2项、湖南省优秀青年科研基金、湖南省优秀博士后基金各1项,先后获省优秀博士研究生学位论文奖、湖南省医学科技一等奖2项,科技进步二等奖1项,医学十大临床创新技术奖1项。主要研究方向为缺血性心脏病的细胞相关治疗研究,以第一或通讯作者身份在国内外学术期刊发表学术论文30余篇,现担任SCI期刊:Journal of the Renin-Angiotensin-Aldosterone System主编、Clinical and Experimental Hypertension主编,Journal of Cardiothoracic Surgery、BMC Bioinformatics副主编,Clinical Case Reports高级主编,European Journal of Medical Research副主编及心脏病学栏目主编,BioMed Research International、PLoS ONE、PeerJ学术主编,BMC Medicine、Reviews in Cardiovascular Medicine、Thoracic and Cardiovascular Surgeon、BMC Cardiovascular Disorders等多本SCI杂志编委。
The Thoracic and Cardiovascular Surgeon Reports (TCS Reports) 为开放获取期刊,出版与胸部和心血管研究具有重要临床相关性的病例报告,特别强调手术介入措施。TCS Reports 欢迎麻醉、心脏病学、生理学和病理学等胸外科和重症监护领域的投稿。
目标与范围
交流有关心脏、血管和胸部手术治疗的特殊或异常病例
报告胸部、血管和心血管手术中治疗管理的临床新方法
记录可能表明对现有疾病病因与发病机制有的新的或替代性理解的特定临床发现
对发表在母刊The Thoracic and Cardiovascular Surgeon上的研究成果和综述进行补充
促进与胸心血管外科护理相关专业和子专业之间更广泛的信息交流
在TCS Reports上的所有投稿均经过严格的同行盲评。鼓励提交图像和视频等补充资料。
