
#Thieme未来星计划荣誉推出神经外科专题,我们将与未来星计划的小伙伴们持续推荐解读与神经外科学相关的论文与研究,欢迎关注。同时,欢迎感兴趣的小伙伴加入我们。
本期推荐 & 解读 BY
亚东 | 首都医科大学
↓ 神经外科专题丨95
前庭神经鞘瘤(VS)是起源于前庭神经、生长缓慢的WHO I级肿瘤。VS大多数呈惰性生长模式,在长期随访期间无进展生长或生长非常缓慢,而相当一部分患者表现出早期的进行性生长。VS周围存在一个复杂的微环境,其特征是炎性细胞浸润,可能与肿瘤进展相关。与生长缓慢或停滞的VS相比,生长快速的VS炎性细胞浸润程度更高,有证据表明,炎性细胞在快速生长的VS微环境中占相当大的比例。VS病理生物学的研究进展为转化研究创造了新的途径,包括早期识别增殖性肿瘤和开发靶向治疗药物。此综述描述并综合了这一研究领域中的关键证据,以及在未来如何影响VS临床管理。通过对PubMed和MEDLINE数据库中“炎症”和“前庭神经鞘瘤”的文献检索,以及对其他来源(包括已发表文章的参考列表)的回顾,确定与VS炎症微环境相关的研究。
J Neurol Surg B Skull Base 2022; 83(01): 001-010
DOI: 10.1055/s-0040-1716688
Review Article
Beyond Antoni: A Surgeon's Guide to the Vestibular Schwannoma Microenvironment
Hannan et al.
中文内容仅供参考,一切以英文原文为准。
结果

图1:巨噬细胞的极性转化及作用。单核细胞/巨噬细胞可以通过Toll样受体(TLR)(如脂多糖(LPS)、干扰素-g(IFN-g)或肿瘤坏死因子-a(TNF-a))极化为M1表型,并分泌促炎细胞因子以抗肿瘤细胞增殖。血管内皮生长因子(VEGF)、白细胞介素-4(IL-4)和白细胞介素-13可将巨噬细胞极化为M2表型,这些细胞分泌的抗炎细胞因子具有促肿瘤作用。CD14和CD68作为巨噬细胞的细胞表面标记物,常见于M1和M2类型。
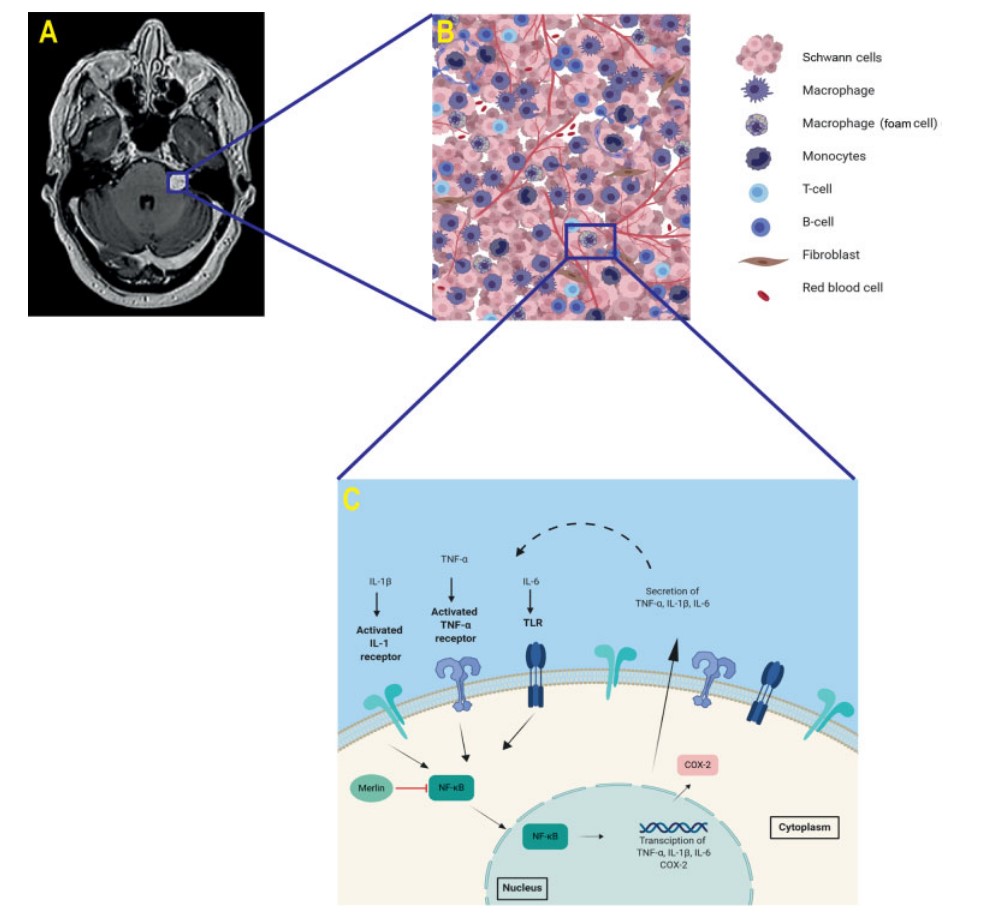
图2: VS生物学行为概述。(A) 轴位增强MRI(B)肿瘤微环境的示意图和与之相关的细胞群(C)炎症反应与细胞因子结合到Schwannoma细胞的表面受体的正反馈通路示意图,激活转录因子NF-κB,可明显上调TNF-α、IL-1β、IL-6和COX-2的表达。细胞骨架肿瘤抑制蛋白merlin阻断NF-κB活性。COX-2的产生受NF-κB的调控。虚线代表正反馈循环,VS内的炎症持续存在。
讨论
自1920年以来,VS中就发现了炎症细胞的存在,尤其是在细胞分布疏松的Antoni B 区。最近,VS炎症细胞浸润的临床意义才开始得到阐明。早期研究对VS患者的炎性细胞浸润进行了半定量分析,并证明炎症水平升高与症状持续时间更长相关。进一步的临床研究证明在较大的VS和生长指数(肿瘤最大直径/患者年龄)升高的肿瘤中,CD45+(泛白细胞标记物)和CD68+(非单核细胞/巨噬细胞标记物)炎性细胞的浸润显著增加。尽管肿瘤生长指数是VS生长速度的粗略度量,但这是第一个将巨噬细胞比例与VS生长联系起来的研究。在一些恶性肿瘤中,炎症反应与肿瘤生长的起始和炎症微环境的维持有关,炎症微环境可促进失调细胞的增殖、血管生成和转移。肿瘤相关巨噬细胞(TAM)已被证明在肿瘤炎症微环境的形成中起关键作用,在许多肿瘤研究中,TAM的存在对治疗和预后有重要影响。例如,在乳腺癌和胰腺癌中,TAM密度越高,预后越差,远处转移的可能性越高。TAM可能在中枢神经系统(CNS)恶性和良性肿瘤的进展中发挥作用。巨噬细胞大致分为M1“经典激活”巨噬细胞和M2“交替激活”巨噬细胞,它们在癌症发病过程中具有不同的功能。M1巨噬细胞以传统抗原呈递巨噬细胞的方式攻击肿瘤细胞,刺激细胞毒性T细胞,吞噬肿瘤细胞,并分泌促炎细胞因子。M2巨噬细胞被认为可以促进肿瘤生长,减弱细胞毒性T细胞反应,促进血管生成,促进细胞外基质的分解,从而促进肿瘤的侵袭和转移。巨噬细胞可以被干扰素-γ和脂多糖诱导为M1表型。相比之下,暴露于免疫调节性细胞因子,如白细胞介素(IL)-4和IL-13,被认为会促使巨噬细胞向致瘤表型发展。许多癌症显示出与M1丰度更高和M2丰度更低存在积极的预后关联。TAM是胶质母细胞瘤微环境的一个特征,许多研究表明,肿瘤促进的M2巨噬细胞比例较高与患者的预后较差之间存在关联。在脑膜瘤中,肿瘤促进型M2巨噬细胞比例较高也可能与组织学分级较高有关。此外,与原发性肿瘤相比,复发性脑膜瘤的特征可能是M2巨噬细胞数量增加。传统认为巨噬细胞在炎症中起核心作用,吞噬病原体,并对微生物制剂和促炎症细胞因子产生反应。巨噬细胞来源并非同质、单一的细胞群,根据刺激表现出不同的反应。在VS中,与缓慢生长的肿瘤相比,在快速生长的肿瘤中观察到更高的表达CD163的M2巨噬细胞浸润。巨噬细胞集落刺激因子(M-CSF)可能在诱导巨噬细胞M2极化中发挥作用,这种细胞因子的表达升高被认为是快速生长的VS的一个特征。CD163+巨噬细胞浸润与更短的无进展生存期之间的关联也已在NF2相关的VS中得到证实。在一项对接受初次次全切除(STR)的VS患者的研究中,切除肿瘤中较高的TAM密度与肿瘤复发和术后面神经功能较差有关。
VS的免疫细胞迁移机制最近被阐明。对切除的VS和正常前庭神经的对比分析显示,在切除的肿瘤中,促炎细胞因子IL-1、IL-6、肿瘤坏死因子-α(TNF-α)和白细胞粘附分子、细胞间粘附分子-1(ICAM-1)的表达增加。此外,最近对60例散发性和NF2相关VS患者标本的分析发现,与来自正常对照神经的Schwannoma细胞相比,VS Schwannoma细胞上的C-X-C趋化因子受体类型4(CXCR4)上调。在小鼠耳蜗移植模型中,VS组织除了在肿瘤本身表达外,还分泌具有耳毒性的促炎性细胞因子,TNF-α是这种耳毒性的介质。
在亚细胞水平上,核因子-κB(NF-κB)是增强VS炎症反应的关键转录因子。核因子-κB(NF-κB)是一种主要的免疫调节因子,由促炎细胞因子如TNF-α和IL-1激活,并控制许多炎症相关基因的表达。在一些恶性肿瘤和VS组织标本中,NF-κB水平被证明上调,它与癌症相关炎症的维持有关。在Schwannoma细胞中,NF-κB活性被merlin抑制,merlin是一种肿瘤抑制蛋白,其缺失对VS的发展至关重要,在衍生VS细胞系中,NF-κB的药理学靶向降低了细胞增殖率。NF-κB激活后,可诱导多种促炎细胞因子的分泌,因此,VS中可能存在自分泌正反馈,由此IL-1和TNF-α激活NF-κB,导致这些促炎细胞因子水平进一步增强。另一个与VS肿瘤内炎症有关的途径是环氧合酶2(COX-2)途径。COX-2是一种在炎症部位上调的酶,其作用是代谢花生四烯酸。COX-2已被发现在包括脑膜瘤在内的多种肿瘤中过度表达,这也适用于VS。COX-2阳性与肿瘤大小和细胞增殖指数呈正相关,通过MIB1表达进行量化。研究发现,COX-2抑制剂可以在体外抑制VS细胞增殖。与NF-κB的情况类似,已知COX-2刺激巨噬细胞产生促炎细胞因子,如IL-1和IL-6,它们本身是COX-2和NF-κB的激活剂。
任何肿瘤的生长都依赖于血管的形成,VS血管生成现已被确定为贝伐单抗药物靶向肿瘤生长的关键驱动因素。在许多实体瘤中,人们认识到TAM丰度和血管密度密切相关,之前对散发性和NF2相关VS的组织学研究也同样证明了这些肿瘤中组织微血管密度、组织血管通透性和TAM密度之间的密切关联。最近对切除的散发性VS和NF2相关VS的组织研究表明,VS TAM是VEGF和VEGFR1表达的来源。然而,越来越多的证据表明,VEGF还可以作为循环中表达VEGFR1的单核细胞的有效化学诱导剂,一旦这些细胞进入肿瘤,VEGF就可以驱动单核细胞向促血管生成和促肿瘤M2巨噬细胞表型发展。肿瘤缺氧和缺氧感应转录因子HIF1α是血管生成和促血管生成细胞因子产生的关键驱动因素,HIF1α在VS中的表达已被证实。在其他肿瘤中,TAM优先定位于缺氧区域,低氧条件促进这些细胞内HIF1α的表达,促使它们向特定的促血管生成激活模式发展。除了刺激血管生成外,HIF1α还被认为通过调节关键趋化因子的表达诱导单核细胞的募集,如CXCL12及其受体CXCR4,并直接影响TAM向原发性M2表型的分化。TAM浸润由此驱动VEGF生成和血管生成,进而促进单核细胞进一步浸润和极化,形成原发性和促血管生成的M2型TAM。然而,目前这一假说的证据是观察性的,需要进一步的体内机制研究来更好地确定VS中血管生成和TAM浸润之间的关系。
临床经验
VS存在复杂的肿瘤微环境,巨噬细胞和其他免疫细胞在VS炎症浸润中的功能格局和作用尚待确定。抗血管生成药物贝伐单抗显示了靶向分子疗法在VS中的疗效。
