

2021年,诺贝尔化学奖授予德国科学家Benjamin List和英裔美籍科学家David W.C. MacMillan,以表彰他们在不对称有机催化发展的贡献。
评委会在颁奖词中表示:“建造分子是一门艰难的艺术。Benjamin List和David W.C. MacMillan因其开发了一种精确的分子构建新工具:有机催化,这对制药研究产生了巨大影响,并使化学变得更加环保。”
作者: 李儒
中科院上海有机所
✦ +
+
Benjamin List
介绍

Benjamin List [本亚明· 利斯特]
德国马克斯·普朗克煤炭研究所(Max-Planck-Institut für Kohlenforschung)所长、德国科学院院士。
Benjamin List教授1968年1月11日出生于德国法兰克福,1993年获柏林自由大学化学学士学位,1997年获法兰克福大学化学博士学位(导师:J. Mulzer),1997-1998年在斯克里普斯研究所(The Scripps Research Institute,TSRI)从事博士后研究,1998-2003年任助理教授。他于2003年加入马克斯·普朗克煤炭研究所,并于2005年起担任“均相催化”系主任,利斯特目前还担任德国科隆大学荣誉教授。他曾于2009年获得汤森路透引文桂冠奖,于2016年获得莱布尼茨奖。
他目前从事“有机小分子催化”方面研究,并且因其在“不对称有机催化的发展”方面的工作而获得2021年诺贝尔化学奖,其与英国化学家戴维·麦克米伦(David W.C. MacMillan)分享了这个奖项。他们的工作对药物研究产生了巨大影响,并使化学更加符合绿色发展的趋势。
✦ +
+
2021年诺贝尔化学奖
Aminocatalysis(不对称有机催化)
Benjamin List在Scripps任职期间,研究了催化抗体用于驱动化学反应(即充当催化剂),他认为酶也能驱动化学反应,并且酶中只有少数氨基酸会参与化学反应。其实在1970年代初就有使用脯氨酸作为催化剂的研究(Hajos-Eder-Sauer-Wiechert反应)[1],但Benjamin List想进一步进行尝试,他测试了脯氨酸是否可以催化羟醛缩合反应,这是一个简单的尝试,但结果却出人意料的好。实验结果不仅证明脯氨酸是一种有效的催化剂,而且证明这种氨基酸可以驱动不对称催化。最终于2000年,Benjamin List与Barbas、Lerner等人报道了脯氨酸催化的不对称羟醛缩合反应(Adol反应)[2](David W.C. MacMillan和他的同事们同时独立地做着类似的工作)。
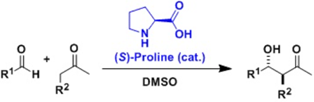
图 1 | 脯氨酸催化的不对称Adol反应
与以往的化学合成同时得到手性分子的两种形式不同,由Benjamin List和David W.C. MacMillan发展的“不对称有机催化”为选择性合成对映体开辟了全新的可能性。自2000年以来,不对称有机催化一直是药物研发和生产的关键部分。由他们分别独立发展的方法,利用结构简单、廉价易设计的有机分子,无需使用对环境有害的重金属即可对映选择性合成重要分子。例如,Benjamin List等人发展的脯氨酸催化的不对称Adol反应后被用于生产HIV药物darunavir。
目前Benjamin List课题组仍在继续探索小分子胺作为羰基转化的不对称催化剂。 “不对称氨基催化”通过使用催化量的胺,将羰基化合物活化为亚胺离子或烯胺中间体参与反应,其策略补充了基于手性酸碱的催化方法(通常涉及金属催化)。在其对2000年第一个不对称脯氨酸催化的分子间醛醇缩合反应研究后,Benjamin List等人意识到烯胺催化有可能成为碳负离子等价物催化反应的普适性策略。从那时起,他们陆续发现其他可用的伯胺或仲胺催化转化反应,并在继续寻找新的胺催化转化反应。
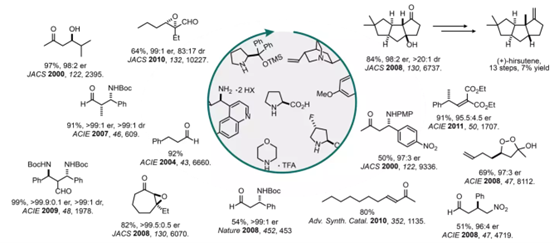
图 2 | 近年来利斯特课题组在“不对称氨基催化”领域的研究进展[3]
例如,2006年Benjamin List在一篇题为“不对称氨基催化的阴阳作用”的综述[4]中总结阐述了烯胺催化亲核加成反应、烯胺催化亲核取代反应以及亚胺催化反应的实例。随后于2008年在《自然》上发表了文章“脯氨酸催化乙醛的Mannich反应”,此反应可以高对映选择性合成具有应用价值的产物[3a],不仅如此利斯特等人目前仍在研究乙醛作为亲核试剂在有机催化Michael反应和aldol反应中的应用。
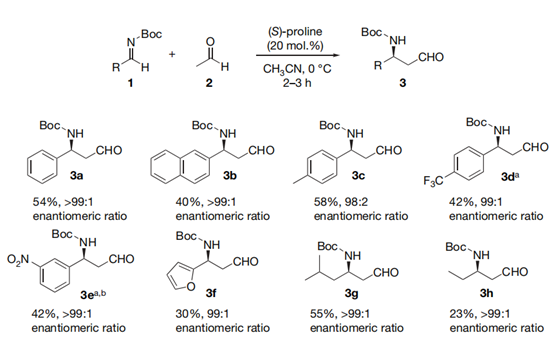
图 3 | 脯氨酸催化乙醛与N-Boc-亚胺的高对映选择性Mannich反应[3a]。
✦ +
+
Brønsted-Acid-Catalysis
Brønsted酸催化反应
而后Benjamin List将目光转移至Brønsted酸催化的反应,目前他的课题组主要集中在手性有机Brønsted酸在不对称反阴离子定向催化[5](ACDC,不对称反阴离子定向催化是指在通过阳离子中间体进行的反应中通过与催化剂提供的手性、对映体纯的阴离子进行离子配对来诱导对映选择性)中的开发和应用。
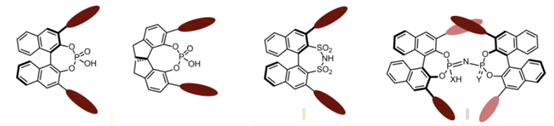
图 4 | 近年来利斯特课题组发展的一系列Brønsted酸催化剂[6]
例如,2005年Benjamin List课题组报道了使用手性磷酸衍生物作为高效有机催化剂,在Hantzsch酯存在下,可高产率、高对映选择性地实现不对称酮亚胺还原加氢反应[6a]。
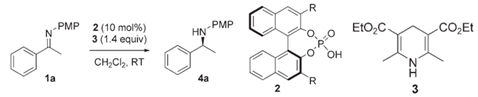
图 5 | 手性磷酸衍生物作为有机催化剂选择性实现不对称酮亚胺还原加氢反应[6a]
2018年,Benjamin List研究小组报道了双轴手性磷酰亚胺催化剂可活化惰性烯烃分子,促使各种1,1-二取代的烯烃底物发生分子内烷氧氢化反应,高对映选择性地得到一系列含季碳中心的α-四氢呋喃化合物[6c]。该方法还可用于(–)-Boivinianin A等生物活性分子的合成,相关工作发表在Science杂志上。
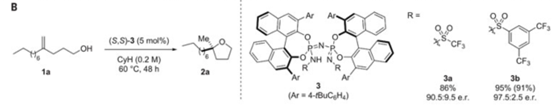
图 6 | 使用双轴手性磷酰亚胺催化剂实现分子内不对称烷氧氢化反应[6c]
2020年,Benjamin List等人在Synlett期刊上报道了最新发展的手性Brønsted酸催化剂,利用此催化剂实现了质子化底物的不对称加成[6d]:高对映选择性二磺酰亚胺(DSI)催化Hantzsch酯还原NH-亚胺盐酸盐(DOI:10.1055/s-0040-1706413)。
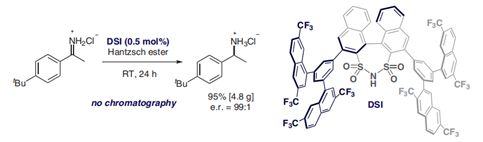
图7 | 高对映选择性二磺酰亚胺催化Hantzsch酯还原NH-亚胺盐酸盐[6d]
✦ +
+
Organic Lewis Acid Catalysis
有机催化剂IDPi
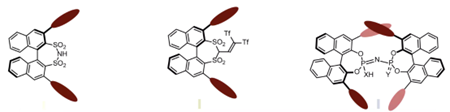

图8 | Brønsted酸与亲核硅烷发生脱硅基化即可原位制备路易斯酸催化剂
2009年,Benjamin List研究小组发展的手性双磺酰亚胺(DSI)催化剂,使手性硅路易斯酸的形成与发展成为了可能。DSI不仅是出色的Brønsted酸,而且在硅烷化时还能形成强路易斯酸,这些原位产生的路易斯酸可促进对映选择性甲硅烷基转移反应[7]。2012年,其发展了新型手性磷酸催化剂IDP[6b],其空间结构具有高度立体诱导催化作用,理论上能够实现惰性底物的不对称反应。但IDP 的酸性(pKa = 11.5 in MeCN)明显低于DSI(pKa = 8.4 in MeCN),这限制了它们在Brønsted酸催化中的适用范围,且手性磷酸的路易斯碱位点与硅正离子无法配位。
之后Benjamin List教授创造性地将DSI与IDP合二为一,互相取长补短,最终得到了强酸性亚氨基二亚磷酸酯(IDPi)催化剂[8a],此催化剂克服了以前的局限性、能够解决该领域长期存在的问题,例如醛的对映选择性 Hosomi-Sakurai 烯丙基化、ppm级催化的不对称Mukaiyama-aldol合成(有机催化负载量的极限)[8b]。近年来Benjamin List研究小组在Synlett等期刊上陆续发表了多种使用IDPi催化剂实现高对映选择性催化的实例[8d-e](例如,DOI:10.1055/a-1670-5829)。
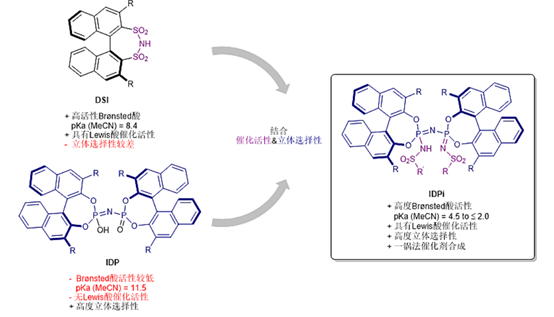
图 9 | 亚氨基二亚磷酸酯(IDPi)催化剂的设计合成
值得一提的是,受Yamamoto和Ghosh等人的启发,Benjamin List课题组于2018年报道了使用乙醛衍生的烯醇硅醚作为亲核底物,实现高度对映选择性的Mukaiyama-aldol合成,有效抑制了反应过程中聚合物的生成。其使用自主开发的超强手性酸IDPi催化剂,与酶一样具有限制的活性位点,同时也和小分子催化剂一样具有广泛的底物范围,对复杂天然药物和生物活性分子的修饰中具有重大的科学意义,相关工作发表在Science上[8c]。
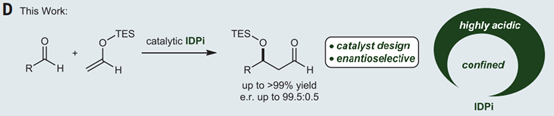
图 10 | 使用超强手性酸IDPi催化剂实现高度对映选择性的Mukaiyama-aldol合成
参考文献:
[1] (a) Z. G. Hajos, D. R. Parrish, J. Org. Chem. 1974, 39, 1615. (b) U. Eder, G. Sauer, R. Wiechert, Angew. Chem., Int. Ed. Engl. 1971, 10, 496. (c) C. Agami, N. Platzer, H. Sevestre, Bull. Soc. Chim. Fr. 1987, 2, 358-360.
[2] B. List, R. A. Lerner, C. F. Barbas III, J. Am. Chem. Soc. 2000, 122, 2395-2396.
[3] (a) J. W. Yang, C. Chandler, M. Stadler, D. Kampen, B. List, Nature 2008, 452, 453–455. (b) B. List, Tetrahedron 2002, 58, 5573-5590. (c) B. List, P. Pojarliev, H. J. Martin, Org. Lett., 2001, 3, 16. (d) B. List, P. Pojarliev, W. T. Biller, H. J. Martin, J. Am. Chem. Soc. 2002, 124, 5. (e) B. List, Acc. Chem. Res. 2004, 37, 548-557.
[4] (a) B. List, Chem. Commun., 2006, 819–824. (b) S. Mukherjee, J. W. Yang, S. Hoffmann, B. List, Chem. Rev. 2007, 107, 5471−5569.
[5] (a) M. Mahlau, B. List, Angew. Chem. Int. Ed. 2013, 52, 518–533. (b) S. L. You, Chem. Asian J. 2007, 2, 820–827. (c) R. M. de Figueiredo, M. Christmann, Eur. J. Org. Chem. 2007, 2575–2600. (d) S. J. Connon, Org. Biomol. Chem. 2007, 5, 3407–3417 etc.
[6] (a) S. Hoffmann, A. M. Seayad, B. List, Angew. Chem. Int. Ed. 2005, 44, 7424 –7427. (b) I. Čorić, B. List, Nature 2012, 483, 315. (c) N. Tsuji, J. L. Kennemur, T. Buyck, S. Lee, S. Prévost, P. S. J. Kaib, D. Bykov, C. Farès, B. List, Science 2018, 359, 1501–1505. (d) V. N. Wakchaure, C. Obradors, B. List, Synlett 2020, 31, A–F.
[7] P. García-García, F. Lay, P. García-García, C. Rabalakos, B. List, Angew. Chem. Int. Ed. 2009, 48, 4363.
[8] (a) P. S. J. Kaib, L. Schreyer, S. Lee, R. Properzi, B. List, Angew. Chem. Int. Ed. 2016, 55, 13200. (b) H. Y. Bae, D. Höfler, P. S. J. Kaib, P. Kasaplar, C. K. De, A. Döhring, S. Lee, K. Kaupmees, I. Leito, B. List, Nat. Chem., 2018, 10, 888-894. (c) L. Schreyer, P.S. J. Kaib, V. N. Wakchaure, C. Obradors, R. Properzi, S. Lee, B. List, Science 2018, 362, 216-219. (d) H. Zhou, P. Zhang, B. List, Synlett 2021, 32, 1953–1956. (e) S. A. Schwengers, C. K. De, O. Grossmann, J. A. A. Grimm, N. R. Sadlowski, G. G. Gerosa, B. List, J. Am. Chem. Soc. 2021, 143, 14835–14844.
扩展阅读
